原子最外层电子数决定了元素的化学性质。
1―20号元素的性质:
1. 氢
氢是元素周期表中的第一号元素,元素名来源于希腊文,原意是“水素”。氢是由英国化学家卡文迪许在1766年发现,称之为可燃空气,并证明它在空气中燃烧生成水。1787年法国化学家拉瓦锡证明氢是一种单质并命名。氢在地壳中的丰度很高,按原子组成占15.4%,但重量仅占1%。在宇宙中,氢是最丰富的元素。在地球上氢主要以化和态存在于水和有机物中。有三种同位素:氕、氘、氚。氢在通常条件下为无色、无味的气体;气体分子由双原子组成;熔点-259.14°C,沸点-252.8°C,临界温度33.19K,临界压力12.98大气压,气体密度0.0899克/升;水溶解度21.4厘米3/千克水(0°C),稍溶于有机溶剂。
在常温下,氢比较不活泼,但可用合适的催化剂使之活化。在高温下,氢是高度活泼的。除稀有气体元素外,几乎所有的元素都能与氢生成化合物。非金属元素的氢化物通常称为某化氢,如卤化氢、硫化氢等;金属元素的氢化物称为金属氢化物,如氢化锂、氢化钙等。
氢是重要的工业原料,又是未来的能源。
2. 氦
元素符号He,原子序数2,原子量4.002602,为稀有气体的一种。元素名来源于希腊文,原意是“太阳”。1868年有人利用分光镜观察太阳表面,发现一条新的黄色谱线,并认为是属于太阳上的某个未知元素,故名氦。后有人用无机酸处理沥青铀矿时得到一种不活泼气体,1895年英国科学家拉姆赛用光谱证明就是氦。以后又陆续从其他矿石、空气和天然气中发现了氦。氦在地壳中的含量极少,在整个宇宙中按质量计占23%,仅次于氢。氦在空气中的含量为0.0005%。氦有两种天然同位素:氦3、氦4,自然界中存在的氦基本上是氦4。氦在通常情况下为无色、无味的气体;熔点-272.2°C(25个大气压),沸点-268.9°C;密度0.1785克/升,临界温度-267.8°C,临界压力2.26大气压;水中溶解度8.61厘米3/千克水。氦是唯一不能在标准大气压下固化的物质。液态氦在温度下降至2.18K时,性质发生突变,成为一种超流体,能沿容器壁向上流动,热传导性为铜的800倍,并变成超导体;其比热容、表面张力、压缩性都是反常的。
氦是最不活泼的元素,基本上不形成什么化合物。氦的应用主要是作为保护气体、气冷式核反应堆的工作流体和超低温冷冻剂。
3. 锂
原子序数3,原子量6.941,是最轻的碱金属元素。元素名来源于希腊文,原意是“石头”。1817年由瑞典科学家阿弗韦聪在分析透锂长石矿时发现。自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷铝石等。在人和动物机体、土壤和矿泉水、可可粉、烟叶、海藻中都能找到锂。天然锂有两种同位素:锂6和锂7。金属锂为一种银白色的轻金属;熔点为180.54°C,沸点1342°C,密度0.534克/厘米3,硬度0.6。金属锂可溶于液氨。
锂与其它碱金属不同,在室温下与水反应比较慢,但能与氮气反应生成黑色的一氮化三锂晶体。锂的弱酸盐都难溶于水。在碱金属氯化物中,只有氯化锂易溶于有机溶剂。锂的挥发性盐的火焰呈深红色,可用此来鉴定锂。 锂很容易与氧、氮、硫等化合,在冶金工业中可用做脱氧剂。锂也可以做铅基合金和铍、镁、铝等轻质合金的成分。锂在原子能工业中有重要用途。
4. 铍
原子序数4,原子量9.012182,是最轻的碱土金属元素。1798年由法国化学家沃克兰对绿柱石和祖母绿进行化学分析时发现。1828年德国化学家维勒和法国化学家比西分别用金属钾还原熔融的氯化铍得到纯铍。其英文名是维勒命名的。铍在地壳中含量为0.001%,主要矿物有绿柱石、硅铍石和金绿宝石。天然铍有三种同位素:铍7、铍8、铍10。铍是钢灰色金属;熔点1283°C,沸点2970°C,密度1.85克/厘米3,铍离子半径0.31埃,比其他金属小得多。
铍的化学性质活泼,能形成致密的表面氧化保护层,即使在红热时,铍在空气中也很稳定。铍即能和稀酸反应,也能溶于强碱,表现出两性。铍的氧化物、卤化物都具有明显的共价性,铍的化合物在水中易分解,铍还能形成聚合物以及具有明显热稳定性的共价化合物。 金属铍主要用作核反应堆的中子减速剂。铍铜合金被用于制造不发生火花的工具,如航空发动机的关键运动部件、精密仪器等。铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。
铍化合物对人体有毒性,是严重的工业公害之一。
5. 硼
原子序数5,原子量10.811。约公元前200年,古埃及、罗马、巴比伦曾用硼沙制造玻璃和焊接黄金。1808年法国化学家盖・吕萨克和泰纳尔分别用金属钾还原硼酸制得单质硼。硼在地壳中的含量为0.001%。天然硼有2种同位素:硼10和硼11,其中硼10最重要。硼为黑色或银灰色固体。晶体硼为黑色,熔点约2300°C,沸点3658°C,密度2.34克/厘米3,硬度仅次于金刚石,较脆。属于非金属元素,符号B
6. 碳
是一种非金属元素,位于元素周期表的第二周期IVA族。拉丁语为Carbonium,意为“煤,木炭”。汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音。碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物――有机物更是生命的根本。碳是生铁、熟铁和钢的成分之一。
碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子。生物体内大多数分子都含有碳元素。碳化合物一般从化石燃料中获得,然后再分离并进一步合成出各种生产生活所需的产品,如乙烯、塑料等。碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等。单质碳的物理和化学性质取决于它的晶体结构。高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等。常温下单质碳的化学性质比较稳定,不溶于水、稀酸、稀碱和有机溶剂;不同高温下与氧反应,生成二氧化碳或一氧化碳;在卤素中只有氟能与单质碳直接反应;在加热下,单质碳较易被酸氧化;在高温下,碳还能与许多金属反应,生成金属碳化物。
7. 氮
原子序数7,原子量为14.006747。元素名来源于希腊文,原意是“硝石”。1772年由瑞典药剂师舍勒和英国化学家卢瑟福同时发现,后由法国科学家拉瓦锡确定是一种元素。氮在地壳中的含量为0.0046%,自然界绝大部分的氮是以单质分子氮气的形式存在于大气中,氮气占空气体积的78%。氮的最重要的矿物是硝酸盐。氮有两种天然同位素:氮14和氮15,其中氮14的丰度为99.625%。
8. 氧
通常条件下呈无色、无臭和无味的气体。密度1.429克/升,1.419克/厘米3(液),1.426克/厘米3(固)。熔点-218.4℃,沸点-182.962℃,化合价一般为0和-2。电离能为13.618电子伏特。除惰性气体外的所有化学元素都能同氧形成化合物。大多数元素在含氧的气氛中加热时可生成氧化物。有许多元素可形成一种以上的氧化物。氧分子在低温下可形成水合晶体O2?H2O和O2?2H2O,后者较不稳定。氧气在空气中的溶解度是:4.89毫升/100毫升水(0℃),是水中生命体的基础。氧在地壳中丰度占第一位。干燥空气中含有20.946%体积的氧;水有88.81%重量的氧组成。除了O16外,还有O17和O18同位素。
9. 氟
原子序数9,原子量18.9984032,元素名来源于其主要矿物萤石的英文名。1812年法国科学家安培指出氢氟酸中含有一种新元素,但自由状态的氟一直没有制得。直到1886年,法国化学家穆瓦桑将氟化钾溶解在无水氢氟酸中进行电解,才制得单质氟。由于氟非常活泼,所以自然界中不存在游离状态的氟。氟在地壳中的含量为0.072%,重要的矿物有萤石、氟磷酸钙等。氟的天然同位素只有氟19。
氟是化学性质最活泼、氧化性最强的物质,氟能同所有其他元素化合;氟与溴、碘、硫、磷、碳、硅等物质在低温下就能猛烈化合;氟离子体积小,容易与许多正离子形成稳定的配位化合物;氟与烃类会发生难以控制的快速反应,氟与NaOH反应:2NaOH+2F2=2NaF+H2O+OF2,氟与水反应:2H2O+2F2 =4HF+O2。
10. 氖(neon)
一种化学元素。化学符号Ne,原子序数10,原子量20.1797,属周期系零族,为稀有气体的成员之一。1898年英国W.拉姆齐和M.W.特拉弗斯在液态空气中发现一种新的稀有气体,取名neon,含义是新奇。氖在地球大气中的含量为18.18×10-4%(体积百分),有3种同位素:氖20、氖21和氖22。氖是无色、无臭、无味的气体,熔点-248.67℃,沸点-245.9℃,气体密度0.9002克/升(0℃,1×105帕),在水中的溶解度10.5微升/千克水。在一般情况下,氖不生成化合物。氖可由液态空气分馏产物经低温选择吸附法制取。氖在放电时发出橘红色辉光,用于制造霓虹灯,还大量用于高能物理研究。
11. 钠
原子序数11,原子量22.989768,是最常见的碱金属元素。元素名来源拉丁文,原意是“天然碱”。1807年英国化学家戴维首先用电解熔融的氢氧化钠的方法制得钠,并命名。在地壳中钠的含量为2.83%,居第六位,主要以钠盐的形式存在。钠是有银白色光泽的软金属,用小刀就能很容易的切割。熔点97.81°C,沸点882.9°C,密度0.97克/厘米3。通常保存在煤油中。
钠是一种活泼的金属。钠与水会产生激烈的反应,生成氢氧化钠和氢;钠还能与钾、锡、锑等金属生成和金;金属钠与汞反应生成汞齐,这种合金是一种活泼的还原剂,在许多时候比纯钠更适用。钠离子能使火焰呈黄色,可用来灵敏地检测钠的存在。 以往金属钠主要用于制造车用汽油的抗暴剂,但由于会污染环境,已经日趋减少。金属钠还用来制取钛,及生产氢氧化钠、氨基钠、氰化钠等。熔融的金属钠在增值反应堆中可做热交换剂。
12. 镁
原子序数12,原子量24.305,为碱土金属中最轻的结构金属。1808年英国化学家戴维通过电解氧华镁和氧化汞的混合物,制得镁汞齐,蒸出其中的汞后,析出金属镁。1828年法国科学家比西用金属钾还原熔融的无水氯化镁得到纯镁。镁在地壳中的含量约2.5%,是第8个最丰富的元素。镁的矿物主要有菱镁矿、橄榄石等。海水中也含有大量的镁。镁也存在于人体和植物中,它是叶绿素的主要组分。 镁为银白色金属;熔点648.8°C,沸点1107°C,密度1.74克/厘米3。镁具有优良的切削加工性能。
金属镁能与大多数非金属和酸反应;在高压下能与氢直接合成氢化镁;镁能与卤化烃或卤化芳烃作用合成格利雅试剂,广泛应用于有机合成。镁具有生成配位化合物的明显倾向。 镁是航空工业的重要材料,镁合金用于制造飞机及森、发动机零件等;镁还用来制造照相和光学仪器等;镁及其合金的非结构应用也很广;镁作为一种强还原剂,还用于钛、锆、铍、铀和铪的生产中。
13. 铝
银白色有光泽金属,密度2.702克/厘米3,熔点660.37℃,沸点2467℃。化合价+3。具有良好的导热性、导电性,和延展性,电离能5.986电子伏特。
虽是叫活泼的金属,但在空气中其表面会形成一层致密的氧化膜,使之不能与氧、水继续作用。在高温下能与氧反应,放出大量热,用此种高反应热,铝可以从其它氧化物中置换金属(铝热法)。例如:8Al+3Fe3O4=4Al2O3+9Fe+795千卡,在高温下铝也同非金属发生反应,亦可溶于酸或碱放出氢气。对水、硫化物,浓硫酸、任何浓度的醋酸,以及一切有机酸类均无作用。
14. 硅
密度:2.33 熔点:1410℃ 沸点:2355℃ 性状:有无定形和晶体两种同素异形体,灰色或黑色。溶解情况:不溶于水、硝酸和盐酸,溶于氢氟酸和碱液。晶型硅单质具有和金刚石类似的空间立体网状结构。所以表现出硬度大,熔点高,质地脆的物理性质,另外硅元素为有周期表的梯形线上,性质介于金属和非金属之间,是灰黑色有金属光泽的半导体。
常温下不活泼,但能与HF反应生成SiF4和H2;能与氢氧化钠溶液反应生成Na3SiO3和H2。加热时与氧反应生成二氧化硅;与氯气反应生成SiCl4;与碳反应生成SiC 。
主要用途:半导体材料,如计算机芯片,新型能源如太阳能电池的硅晶板
15. 磷
单质磷有几种同素异形体。其中,白磷或黄磷是无色或淡黄色的透明结晶固体。密度1.82克/厘米3。熔点44.1℃,沸点280℃,着火点是40℃。放于暗处有磷光发出。有恶臭。剧毒。白磷几乎不溶于水,易溶解与二硫化碳溶剂中.在高压下加热会变为黑磷,其密度2.70克/厘米3,略显金属性。电离能为10.486电子伏特。不溶于普通溶剂中。白磷经放置或在400℃密闭加热数小时可转化为红磷。红磷是红棕色粉末,无毒,密度2.34克/厘米3,熔点59℃,沸点200℃,着火点240℃。不溶于水。在自然界中,磷以磷酸盐的形式存在,是生命体的重要元素。存在于细胞、蛋白质、骨骼和牙齿中。在含磷化合物中,磷原子通过氧原子而和别的原子或基团相联结
16.硫
通常为淡黄色晶体,它的元素名来源于拉丁文,原意是鲜黄色。单质硫有几种同素异形体,菱形硫(斜方硫)和单斜硫是现在已知最重要的晶状硫。它们都是由S8环状分子组成。
密度 熔点 沸点 存在条件
菱形硫(S8)2.07克/厘米3 112.8℃ 444.674℃ 200℃以下
单斜硫(S8)1.96克/厘米3 119.0℃ 444.6℃ 200℃
以上硫单质导热性和导电性都差。性松脆,不溶于水,易溶于二硫化碳(弹性硫只能部分溶解)。无定形硫主要有弹性硫,是由熔态硫迅速倾倒在冰水中所得。不稳定,可转变为晶状硫(正交硫),正交硫是室温下唯一稳定的硫的存在形式。
17.氯
常温常压下为黄绿色气体。密度3.214克/升。熔点-100.98℃,沸点-34.6℃。化合价-1、+1、+3、+5和+7。有毒,剧烈窒息性臭味。电离能12.967电子伏特,具有强的氧化能力,能与有机物和无机物进行取代和加成反应;同许多金属和非金属能直接起反应。
18. 氩
其是单原子分子,单质为无色、无臭和无味的气体。是稀有气体中在空气中含量最多的一个,100升空气中约含有934毫升。密度1.784克/升。熔点-189.2℃。沸点-185.7度。电离能为15.759电子伏特。化学性极不活泼,按化合物这个词的一般意义来说,它是不会形成任何化合物的。氩不能燃烧,也不能助燃。
19. 钾
原子序数19,原子量39.0983。元素名来源于拉丁文,原意是“碱”。1807年由英国化学家戴维首次用电解法从氢氧化钾熔体中制得金属钾,并定名。钾在地壳中的含量是2.59%,居第七位。重要的价矿物有钾石盐、钾硝石等;海水中含有氯化钾,其含量为氯化钠的1/40;土壤中的钾很容易进入植物组织,所以植物灰中都含有碳酸钾。钾有三种天然同位素:钾39、钾40和钾41。钾是一种轻而软的低熔点金属;熔点为63.25°C,沸点760°C,密度0.86可/厘米3。
钾比钠活泼,金属钾与水或冰的反应,即使温度低到-100°C,也非常剧烈;与酸的水溶液反应更为剧烈。金属钾在空气中燃烧,易生成橘红色的超氧化钾。金属钾与氢气反应很慢,但在400°C时反应很快。金属钾与一氧化碳反应能生成一种爆炸性的羰基化合物。含钾的化合物能使火焰呈现紫色。 钾盐是重要的肥料,是植物生长的三大营养元素之一。
20. 钙
原子序数20,原子量40.078,是碱土金属中最活泼的元素。元素名来源于拉丁文,愿意为“石灰”。1808年英国化学家戴维在电解石灰和氧化汞的混合物时得到钙汞齐,然后蒸掉汞制得纯的金属钙。钙在地壳中的含量为3.64%,排第5位。钙以化合物的形式广泛存在于自然界中,钙的主要矿物有石灰石、方解石、大理石等。 钙呈银白色;熔点839°C,沸点1484°C,密度1.54克/厘米3。
钙的氧化态为+2,它能同空气中的氧和氮缓慢作用生成一层氧化物和氮化物保护膜;钙与冷水作用缓慢,在热水中发生剧烈反应放出氢;钙可与卤族元素直接反应,在加热下与硫、碳反应;钙与浓氨水形成六氨合钙,这是一种有金属光泽的高导电性固体。
钙在生物体中是一种重要的元素。动物体内的钙不仅参加骨骼和牙齿的组成,而且参与新陈代谢。
相关初中化学知识点:化学式的写法和意义
概念:
用元素符号和数字的组合表示物质组成的式子,叫做化学式。如可用O2,H2O,MgO分别表示氧气、水、氧化镁的化学式。
对概念的理解:
(1)混合物不能用化学式表示,只有纯净物才能用化学式表示。
(2)每一种纯净物只有一个化学式,但一个化学式有可能用来表示不同的物质。如氧气的化学式是O2,没有别的式子再能表示氧气;P既是红磷的化学式,也是白磷的化学式。
(3)纯净物的化学式不能臆造,化学式可通过以下途径确定:
①科学家通过进行精确的定量实验,测定纯净物中各元素的质量比,再经计算得出。
②已经确定存在的物质可根据化合价写出。
书写规则:
1.单质化学式的写法:
首先写出组成单质的元素符号,再在元素符号右下角用数字写出构成一个单质分子的原子个数。稀有气体是由原子直接构成的,通常就用元素符号来表示它们的化学式。金属单质和固态非金属单质的结构比较复杂,习惯上也用元素符号来表示它们的化学式。
2.化合物化学式的写法:
首先按正前负后的顺序写出组成化合物的所有元素符号,然后在每种元素符号的右下角用数字写出每个化合物分子中该元素的原子个数。一定顺序通常是指:氧元素与另一元素组成的化合物,一般要把氧元素符号写在右边;氢元素与另一元素组成的化合物,一般要把氢元素符号写在左边;金属元素、氢元素与非金属元素组成的化合物,一般要把非金属元素符号写在右边。直接由离子构成的化合物,其化学式常用其离子最简单整数比表示。
化学式的读法:
一般是从右向左叫做“某化某”,如“CuO”叫氧化铜。当一个分子中原子个数不止一个时,还要指出一个分子里元素的原子个数,如“P2O5”叫五氧化二磷。有带酸的原子团要读成“某酸某”如“CuSO4”叫硫酸铜,还有的要读“氢氧化某”,如“NaOH”叫氢氧化钠。“氢氧化某”是碱类物质,电离出来的负电荷只有氢氧根离子。
化学式的意义:
(1)由分子构成的物质
| 化学式的含义 | 以H2O为例 | ||
| 质的含义 | 宏观 | ①表示一种物质 ②表示物质的元素组成 | ①表示水 ②表示水是由氢、氧两种元素组成的 |
| 微观 | ①表示物质的一个分子 ②表示组成物质每个分子的原子种类和数目 ③表示物质的一个分子中的原子总数 | ①表示一个水分子 ②表示一个水分子是由两个氧原子和一个氧原子构成的 ③表示一个水分子中含有三个原子 | |
| 量的含义 | ①表示物质的相对分子质量 ②表示组成物质的各元素的质量比 ③表示物质中各元素的质量分数 | ①H2O的相对分子质R =18 ②H2O中氢元素和氧元素质量比为1:8 ③H2O中氢元素的质量分数= 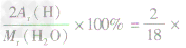 100%=11.1% 100%=11.1% | |
(2)由原子构成的物质(以Cu为例)
宏观:
表示该物质:铜
表示该物质由什么元素组成:铜由铜元素组成
微观:表示该物质的一个原子―一个铜原子。
化学式和化合价的关系:
(1)根据化学式求化合价
①已知物质的化学式,根据化合价中各元素的正负化合价代数和为0的原则确定元素的化合价。
标出已知、未知化合价: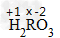
列出式子求解:(+1)×2+x×1+(-2)×3=0 x=+4
②根据化合价原则,判断化学式的正误,如判断化学式KCO3是否正确
标出元素或原子团的化合价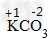
计算正负化合价代数和是否为0:(+1)×1+(-2)×1=-1≠0,所以给出的化学式是错误的,正确的为K2CO3。
③根据化合价原则,计算原子团中某元素的化合价,如计算NH4+中氮元素的化合价和H2PO4-(磷酸二氢根)中磷元素的化合价。
由于NH4+带一个单位的正电荷,不是电中性的,因此各元素的化合价代数和不为多,而是等于+1. 设氮元素的化合价为x
x+(+1)×4=+1 x=-3
所以在NH4+中,氮元素的化合价为-3. 同理H2PO4-带一个单位的负电荷、不是电中性的、因此各元素的化合价代数和不为零,而是-1.
设磷元素的化合价为y
(+1)×2+y+(-2)×4=-1 y=+5 所以在H2PO4-中磷元素的化合价为+5.
④根据化合价原则,确定物质按化合价的排序。如H2S,S,SO2,H2SO4四种物质中均含有硫元素,并且硫元素的化合价在四种物质中分别为:-2,0, +4,+6,故这四种物质是按硫元素的化合价由低到高的顺序排列的。
(2)根据化合价写化学式
根据化合物中化合价的代数和等于0的原则,已知元素的化合价可以推求实际存在物质的化学式,主要方法有两种:
①最小公倍数法
| 步骤 | 举例 | |
| 写 | 一般把正价元素的符号(或原子团)写在左边,负价元素的符号(或原子团)写在右边,并把化合价写在元素符号(或原子团)的正上方 | 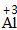 、 、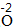 |
| 求 | 求出两种元素化合价绝对位的最小公倍数,然后求出每种元素的原子个数= | 因为|-2|×|+3|=6,所以Al原子个数为6/3=2,O原子个数=6/2=3 |
| 标 | 将原子个数写在相应元素符号的正下角 | Al2O3 |
| 验 | 检验各种元素正负化合价的代数和是否为0,确定化学式的正确性 | (+3)×2+(-2)×3=0,所以该化学式正确。 |
| 步骤 | 例1 硫酸铜 | 例2 氧化钙 | |
| 排列 | 分析名称,确定元素符号(或原子团)的顺序 | 铝 硫酸根 Al SO4 | 钙 氧 Ca O |
| 标价 | 标上化合价 | 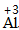 、 、 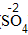 | 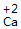 、 、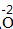 |
| 约简 | 将化合价的绝对值约成最简整数比 | 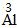 、 、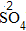 | 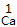 、 、 |
| 交叉 | 将整数交叉写在元素符号(或原子团)的右下角 |  |  |
| 检验 | 根据正负化合价代数和是否为0,检验正误 | (+3)×2+(-2)×3=0 | (+2)+(-2)=0 |
确定化学式的几种方法:
1. 根据化合价规则确定化学式
例1:若A元素的化合价为+m,B元素的化合价为-n,已知m与n都为质数,求A,B两元素化合后的物质的化学式。
解析:由题意知正、负化合价的最小公倍数为m ・n,A的原子个数为(m・n)/m=n,B的原子个数为 (m・n)/n=m
答案:所求化学式为AnBm.
2. 根据质量守恒定律确定化学式
例2:根据反应方程式2XY+Y2==2Z,确定Z 的化学式
解析:根据质量守恒定律,反应前后原子种类不变,原子数目没有增减,反应前有两个X原子,四个Y原子,则两个Z分子含有两个X原子和四个Y原子。
答案:z的化学式为XY2
3. 利用原子结构特征确定化学式
例3:X元素的原子核外有17个电子,Y元素的原子最外层有2个电子,求X、Y两元素所形成的化合物的化学式。
解析:X元素的原子核外有17个电子,Y元素的原子最外层有2个电子,X原子易得1个电子,Y原子易失2个电子,根据电子得失相等可求化合物的化学式为YX2
4.利用元素质量比确定化学式:
例4:有一氮的氧化物,氮、氧两元素的质量比为7: 4,求此氧化物的化学式。
解析:设此氧化物的化学式为NxOy,根据xN:yO =7:4 得14x:16y=7:4,即x:y=2:1。
答案:所求氧化物的化学式为N2O。
5. 利用化学式中所含原子数、电子数确定化学式
例5:某氮氧化合物分子中含有3个原子,23个电子,求此化合物的化学式。
解析:设此化合物的化学式为NxOy,则
x+y=3
7x+8y=23
解得x=1,y=2
答案:所求化学式NO2。
利用化学式的变形比较元素的原子个数:
例:质量相等的SO2和SO3分子中,所含氧原子的个数比为?
解析:SO2的相对分子质量为64,SO3的相对分子质量为80,二者的最小公倍数是320,二者相对分子质量相等时物质的质量相同,转化为分子个数SO2 为320/64=5,SO3为320/80=4,即5SO2与4SO3质量相同,所以含氧原子的个数比为(5×2):(4×3)=10:12=5:6。
四、利用守恒法进行化学式计算:
例:由Na2S、Na2SO3、Na2SO4三种物质构成的混合物中,硫元素的质量分数为32%,则混合物中氧元素的质量分数为?
解析:在Na2S,Na2SO3,Na2SO4中,钠原子与硫原子的个数比是恒定的,都是2:1,因而混合物中钠、硫元素的质量比(或质量分数比)也是恒定的。设混合物中钠元素的质量分数为x,可建立如下关系式。
Na ――S
46 32
x 32%
46/32=x/32%
解得x=46%
混合物中氧元素的质量分数为1-32%-46%=22%。
利用平均值法判断混合物的组成
找出混合物中各组分的平均值(包括平均相对原子质量、平均相对分子质量、平均质量、平均质量分数等),再根据数学上的平均值原理,此平均值总是介于组成中对应值的最大值与最小值之间,由此对混合物的组分进行推理判断。
例:某气休可能由初中化学中常见的一种或多种气体组成,经测定其中只含C,O两种元素,其质量比为3:8,则该气体可能是?
解析:由题给条件知,该气体只含C,O两种元素,而这两种元素组成的气体可能是CO2、CO,O2。CO2中C,O两种元素的质量比是3:8,CO中C,O两种元素的质量比是3:4,O2中C,O两种元素的质量比是0 (因C的质量为0)。题中给出该气体中C,O两种元素的质量比是3:8,故符合题意的气体组成为:CO2或 CO,O2或CO,O2,CO2。
利用关系式法解题技巧:
关系式法是根据化学式所包含的各种比例关系,找出已知量之间的比例关系,直接列比例式进行计算的方法。
例: 多少克(NH4)2SO4与42.4g尿素CO(NH2)2所含的氮元素质量相等?
设与42.4g尿素中所含氮元素质量相等的(NH4)2SO4的质量为x
(NH4)2SO4――2N――CO(NH2)2
132 60
x 42.4g
132/x=60/42.4g
x=93.28
化学式前和化学式中数字的含义:
①化学式前面的数字表示粒子(原子、分子)数目;
②离子符号前的数字表示离子的数目;
③化学式石一下角的数字表示该粒子中对应原子或原子团的数目;
④离子符号右上角的数字表示该离子所带电荷数。

相关初中化学知识点:化合价的求法
求化合价:
化合价是元素的一种性质,它只有在元素彼此化合时才表现出来。在化合物中正、负化合价代数和等于零,这是求化合价的准则。
几种求法:
一、由化学式或根式
1.求AmBn化合物中A元素化合价的公式: (B元素的化合价×B的原子个数)/A的原子个数
2.求多元化合物中未知化合价的元素的化合价公式: (已知化合价诸元素价数的代数和)/未知化合价的元素的原子个数
3.根据正、负电荷数判断元素(或原子团)的化合价。 在根式中,正、负化合价总价数的代数和等于根式所带的正、负电荷数。
二、由元素质量比
1.(A元素的相对原子质量×B元素的化合价)/(B元素的相对原子质量×元素的化合价)=A元素的质量比值/B元素的质量比值
2.A元素的质量比值(或百分组成)×A的化合价/A的相对原子质量=B元素的质量比值(或百分比组成)×B的化合价/B相对原子质量
三、由质量比
(B的化合价×A的相对原子质量比值)/(A的化合价×B的相对原子质量比值)=A元素的质量比值/B元素的质量比值
正负代化合价数和为零:
【例1】试确定化合物K2MnO4中Mn元素的化合价。 解析:设化合物中Mn元素化合价为+x价,依化合物中各元素化合价正负代数和为零的原则有2×(+1)+1×(+x)+4×(-2)=0解之得x=6 故K2MnO4中Mn元素化合价为+6价。
电子层结构法
【例2】元素X的原子最外层上有1个电子,元素Y的原子最外层上有6个电子,则X、Y两元素可形成的化合物的化学式为[] A.XYB.X2YC.XY2D.X3Y 解析:本题的关键可以说是首先得确定在形成化合物时,X、Y两元素所表现的化合价。因X最外层上只有1个电子,最高正价为+1价,Y最外层6个电子,离8电子稳定结构尚差2个,故最低负价为-2价,则X、Y所形成化合物分子式为X2Y,应选B。
质量分数法
【例3】某元素的相对原子质量为59,在其氧化物中该元素的质量分数为71%,则它的化合价为[] A.+1B.+2C.+3D.+4 解析:设该元素的氧化物化学式为RxOy 依题意有59x/(59x+16y)*100%=71% 解得x/y=2:3 故化学式为R2O3,R化合价为+3价,选C。
质量守恒定律法
【例4】某金属氧化物与足量的盐酸反应,生成的氯化物与水的分子数之比为2∶3,则该金属的化合价是[] A.+1B.+2C.+3D.+4
解析:设生成的氯化物化学式为RClx,依题意有分子数之比RClx∶H2O=2∶3根据质量守恒定律可知,反应前后各元素的原子种类和数目不变,生成物中H、Cl的原子个数比也应为1:1,故x值为3,则R的化合价为+3价,选C。
相对分子质量法
【例5】某金属元素的氧化物相对分子质量为M,同价态的氯化物相对分子质量为N,则该元素的化合价数值为[]
解析:设该元素化合价为+x价,相对原子质量为MR
(1)如x为奇数时,氧化物化学式为R2Ox,氯化物化学式为RClx,据题意有
2MR+16x=M(1)
MR+35.5x=N(2)
(2)*2-(1)得x的值为x=+(2N-M)/55
(2)x为偶数时,氧化物化学式为Rox/2氯化物化学式为RClx,据题意有 MR+35.5x=N(4) x=+(N-M)/27.5
质量关系法
【例6】相对原子质量为M的金属单质ag与足量的稀硫酸反应,产生bg氢气,则反应中该金属元素的化合价为[]
解析:设金属在反应中化合价为+x价,则金属单质与生成H2有如下关系:
2R~xH2
2M 2x
a b
故应选B。
相关因素讨论法
【例7】某元素M原子最外层电子数少于5,其氧化物化学式为MxOy,氯化物化学式MClz当y∶z=1∶2时,M的化合价可能是[]
A.+1B.+2C.+3D.+4
解析:M的化合价在数值上等于z的值
如y=1z=2(合理) y=2z=4(合理) y=3z=6(与最外层电子数少于5不符) 故应选B、D。
本文来自:逍遥右脑记忆 /chuzhong/258167.html
相关阅读:初中课外化学实验 检验含碘食盐成分中的碘
关于乐果的初中化学知识百科
初中化学?电木的来历
德国化学家?瓦拉赫
瑞典
